欢迎关注我的CSDN:https://spike.blog.csdn.net/
本文地址:https://spike.blog.csdn.net/article/details/136302202

大分子药物设计领域主要包括3个方面,即大环类药物设计、蛋白质与多肽类药物设计、核酸药物设计等,具体如下:
-
大环类药物设计:是指利用具有大环结构的化合物作为药物候选分子或先导化合物的设计策略。大环结构可以提高药物的亲和力、渗透性、稳定性和选择性,同时可以作用于难以成药的靶点,如蛋白-蛋白相互作用。大环类药物的设计需要考虑大环的形成、尺寸、构象和元素组成等因素,以及与靶点的结合模式和动力学。大环类药物的合成也是一个挑战,需要选择合适的关环反应和条件。
-
蛋白质与多肽类药物设计:是指利用具有蛋白质或多肽结构的生物大分子作为药物候选分子或先导化合物的设计策略。蛋白质与多肽类药物具有高度的特异性和生物活性,可以模拟或调节生理过程中的信号分子,如激素、生长因子、抗体等。蛋白质与多肽类药物的设计需要考虑蛋白质或多肽的序列、结构、稳定性、可溶性、半衰期和免疫原性等因素,以及与靶点的结合模式和动力学。蛋白质与多肽类药物的合成可以采用化学或生物技术的方法,如固相合成、酶催化、基因工程等。
-
核酸药物设计:是指利用具有核酸结构的生物大分子作为药物候选分子或先导化合物的设计策略。核酸药物可以通过与靶标RNA或DNA进行杂交或结合,从而调控基因的表达或编辑。核酸药物的种类包括寡核苷酸药物(如siRNA、miRNA、antisense oligo等)和核糖核酸药物(如mRNA、CRISPR RNA等)。核酸药物的设计需要考虑核酸的序列、结构、稳定性、递送系统和毒性等因素,以及与靶标的结合模式和动力学。核酸药物的合成可以采用化学或生物技术的方法,如固相合成、酶催化、转录等。
1. 大环类药物设计
大环类药物是指分子中含有至少一个大于12个原子的环的化合物,具有一些特殊的理化和生物学性质,例如:
- 可以提高药物与靶标的亲和力和选择性,因为大环结构可以限制分子的构象自由度,减少熵损失,增强分子间的相互作用。
- 可以改善药物的渗透性和稳定性,因为大环结构可以根据环境的极性调整自身极性,掩埋和屏蔽部分极性基团,降低极性表面积,从而适应不同的生物屏障。同时,大环结构也可以抵抗酶的水解和代谢,延长药物的体内半衰期。
- 可以作用于难以成药的靶标,如蛋白-蛋白相互作用,因为大环结构可以模拟天然的肽或蛋白片段,与靶标蛋白的大型结合口袋相匹配,突破Lipinski规则的限制。
大环类药物在药物设计中的应用场景很广泛,包括抗感染、抗癌、免疫调节、神经系统等领域。已经上市或正在临床试验的大环药物的例子有:
- 奥波佐米(Oprozomib),口服的大环类药物,用于治疗多发性骨髓瘤,蛋白酶体抑制剂,可以阻断恶性细胞的蛋白降解途径,诱导细胞凋亡,目前处于Ⅱ期临床试验。
- 奥马西汀(Omadacycline),静脉或口服的大环类药物,用于治疗社区获得性肺炎和皮肤感染,四环素类抗生素,可以抑制细菌的蛋白质合成,具有广谱的抗菌活性,已经于2018年获得美国FDA的批准。
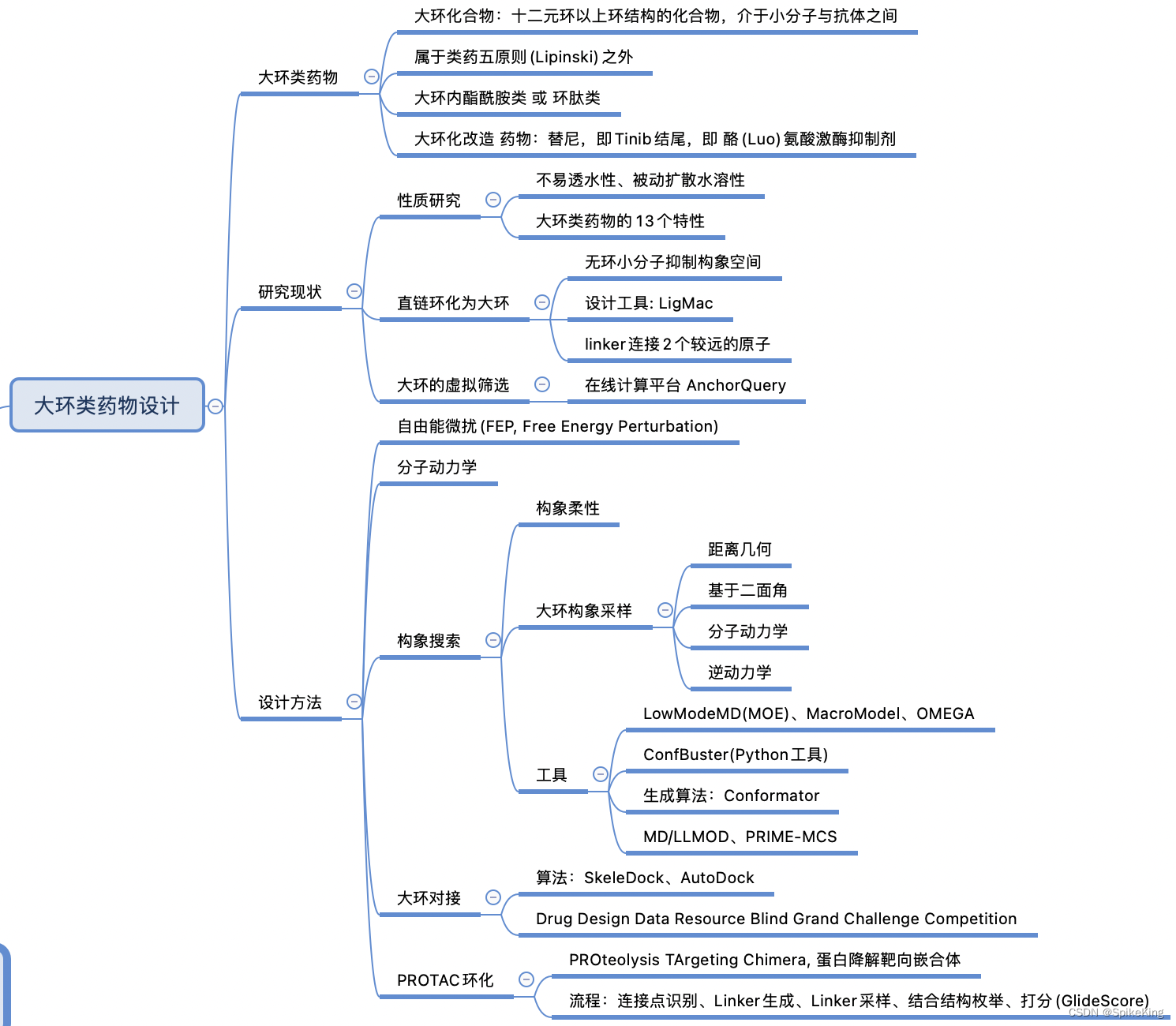
替尼类药物,即Tinib结尾,即Tyrosine Kinase Inhibitons,酪(Luo)氨酸激酶抑制剂。酪氨酸激酶抑制剂是一类能抑制酪氨酸激酶活性的化合物,已经开发为数种抗肿瘤药物。酪氨酸激酶抑制剂主要通过抑制细胞信号转导而抑制肿瘤细胞的生长和增殖,促进细胞凋亡。
2. 蛋白质与多肽类药物设计
蛋白质与多肽类药物设计的要点主要包括以下几个方面:
- 目标选择:根据疾病的机理和靶点的特性,选择合适的蛋白质或多肽作为药物候选物。
- 多肽合成:通过化学或生物技术的方法,合成所需的蛋白质或多肽分子,或者对其进行修饰以改善其稳定性、溶解性、半衰期等性质。
- 药物筛选:通过体外和体内的实验,评估药物的活性、选择性、毒性、药代动力学等参数,筛选出最优的药物候选物。
- 药物优化:通过结构优化、剂型优化、给药途径优化等手段,提高药物的效果、安全性、便利性等指标,使其符合临床要求。
蛋白质与多肽类药物设计的应用场景非常广泛,目前已有超过80种蛋白质与多肽类药物上市,涵盖了内分泌、免疫、神经、肿瘤等多个领域。例如:
- 胰岛素:一种用于治疗糖尿病的多肽药物,可以降低血糖水平,模拟人体内的胰岛素功能。
- 赫赛汀:一种用于治疗HER2阳性乳腺癌的单克隆抗体药物,可以与HER2受体结合,阻断其信号传导,抑制肿瘤细胞的增殖和存活。
- 骨形成蛋白:一种用于治疗骨质疏松症的蛋白质药物,可以刺激骨前体细胞的分化,促进骨组织的形成和修复。

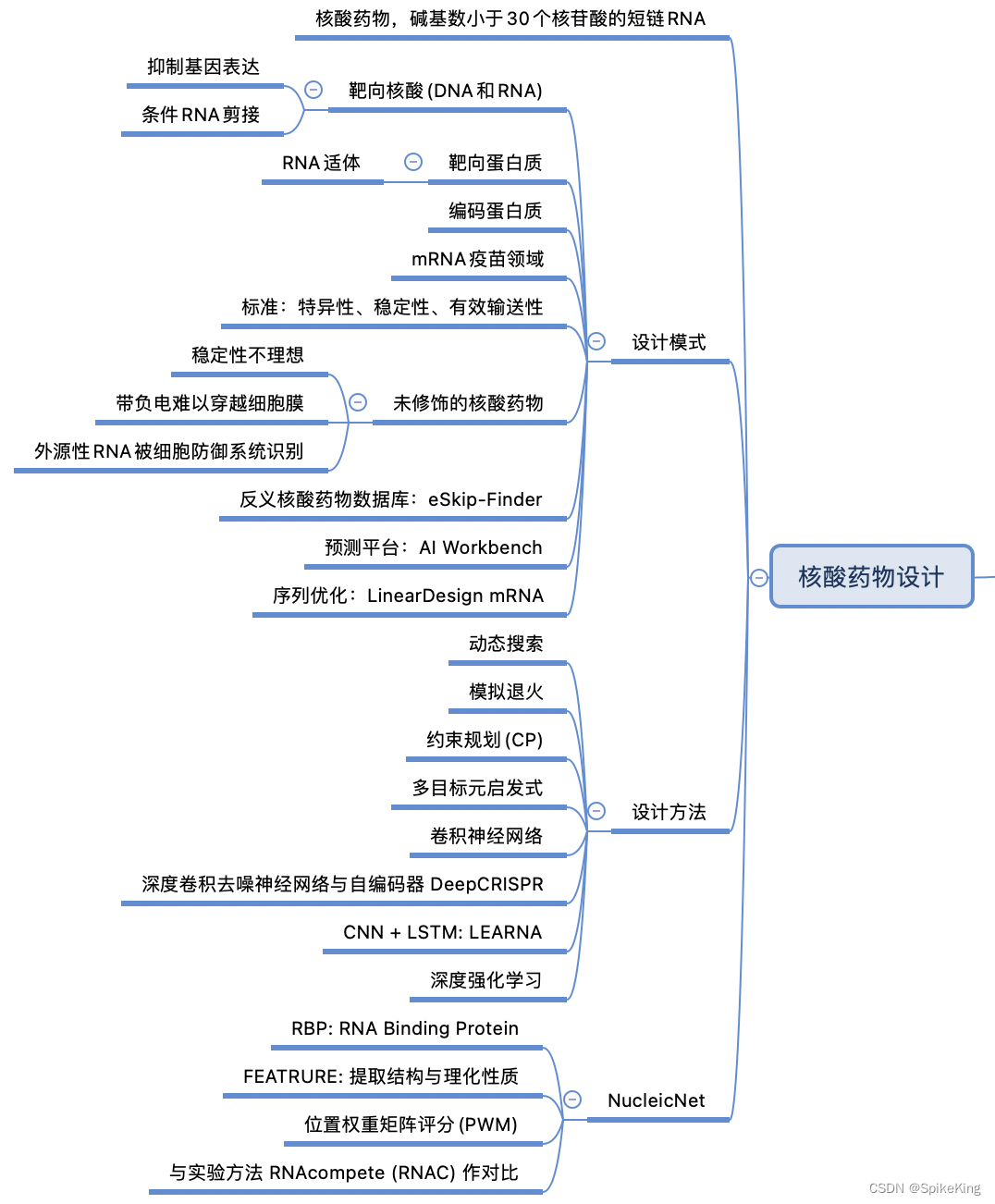
3. 核酸药物设计
核酸药物是一类利用核酸分子作为药物或药物载体的新型药物,可以通过调节基因表达来治疗各种疾病。核酸药物的主要分类有:
- 反义核酸(Antisense Oligonucleotides, ASO):与靶基因的mRNA互补的单链核酸分子,可以通过杂交、降解或阻断mRNA的翻译来抑制基因的表达。
- 小干扰RNA(Small Interfering RNA, siRNA):由两条互补的单链 RNA 组成的双链RNA分子,可以通过RNA干扰(RNA interference, RNAi)机制,引导 RISC 复合物切割与之互补的mRNA,从而降低基因的表达。
- 信使RNA(Messenger RNA, mRNA):是一种携带遗传信息的单链RNA分子,可以通过转录后修饰和包裹技术,被送入细胞内,作为蛋白质的模板进行翻译,从而增加基因的表达。
核酸药物具有高度的特异性、选择性和效力,可以针对难以成药的靶点和疾病,具有广阔的应用前景。
核酸药物设计是一种利用核酸分子(如DNA或RNA)作为药物的策略,通过与疾病相关的基因或蛋白质相互作用,调节其表达或功能,从而达到治疗或预防的目的。核酸药物设计的要点包括:
- 核酸药物的选择:根据药物的作用机制和靶点,选择合适的核酸分子类型,如siRNA、miRNA、antisense oligo、mRNA、CRISPR RNA等。
- 核酸药物的设计:根据核酸药物的特性和需求,进行序列优化、化学修饰、结构设计等,提高药物的稳定性、亲和力、特异性、效率和安全性。
- 核酸药物的递送:根据核酸药物的目标组织和细胞,选择合适的递送系统,如脂质体、纳米粒子、病毒载体等,增强药物的生物利用度、细胞内转运和释放。
核酸药物设计的应用场景非常广泛,理论上,任何由基因异常引起的疾病都可以通过核酸药物进行治疗或预防,如癌症、遗传性疾病、感染性疾病、代谢性疾病等。目前,已有多种核酸药物进入临床试验或上市,如Nusinersen(治疗脊髓性肌萎缩症)、Patisiran(治疗遗传性淀粉样变性)、Moderna的mRNA疫苗(预防新冠病毒感染)等。核酸药物设计是药物研发领域的一个重要方向,具有巨大的潜力和前景。